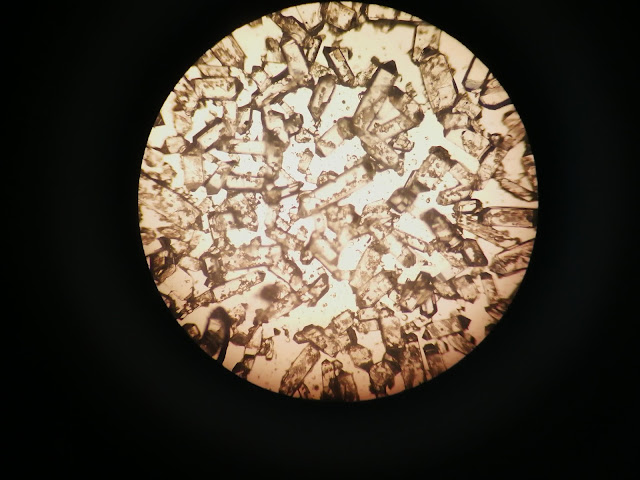
Como ya se indicado anteriormente, el cristal y el vidrio no son lo mismo. La gran diferencia: EL ORDEN. El cristal es un sólido homogéneo formado por partículas perfectamente ordenadas debido a su crecimiento lento. El vidrio por contra, es un sólido homogéneo formado por partículas dispuestas al azar. Para representar esta diferencia vamos a usar el azúcar.
En entradas anteriores hemos preparado cristales de azúcar y geodas de azúcar. Ambas estructuras cristalinas de azúcar que han tardado entre 2 y 4 semanas en formarse. Ahora nos disponemos a preparar vidrio de azúcar con el diseño de una vidriera. Para ello seguiremos el siguiente procedimiento:
1) En un bol se mezclan un vaso de azúcar, medio vaso jarabe de maíz y 0´5 g de cremor tártaro.
2) Se cubre con film transparente
3) Se calienta a máxima potencia en un microondas durante 3 minutos
4) Se retira el film transparente con cuidado de que no caiga agua sobre el azúcar. Se sustituye por otro film transparente. Esta etapa puede ser peligrosa por vapor que sale a elevada temperatura. Tener especial cuidado y usar protección. Se puede abrir un agujero con un cuchillo para que escape el vapor antes de retirar el film.
5) Se vuelve a calentar en el microondas, esta vez 4 minutos. Se deben superar los 186ºC (punto de fusión del azúcar). Si no tenemos termómetro, se puede comprobar dejando caer una gota en un vaso con agua y se observa que deja un hilo en el agua la gota.
6) Se retira el film transparente (mismo cuidado que en etapa 4).
7) Se añade colorante alimentario si se desea agitando hasta aspecto homogéneo. Este proceso debe de ser rápido.
7) Se añade colorante alimentario si se desea agitando hasta aspecto homogéneo. Este proceso debe de ser rápido.
7) Se añade al molde que se desee y se deja enfriar sobre papel de horno.
Repitiendo varias veces el proceso para dar distintos colores hemos acabado por crear nuestra vidriera.